Mettre fin au non-sens
 Des ARN de transfert modifiés neutralisent l'effet de variants génétiques « non-sens » qui introduisent un codon stop indésirable (appelé codon de terminaison prématurée, ou PTC) là où devrait se trouver un codon habituel.
Des ARN de transfert modifiés neutralisent l'effet de variants génétiques « non-sens » qui introduisent un codon stop indésirable (appelé codon de terminaison prématurée, ou PTC) là où devrait se trouver un codon habituel.
La méthode repose sur la synthèse d'ARNt modifiés (ARTNt suppresseurs sup-tRNA en anglais) qui se fixent sur l'ARNm au niveau du PTC et apportent un acide aminé qui permet la poursuite de la traduction en une protéine de longueur complète. La figure 2 de Keeling (2025) décrit le principe du mécanisme d'action des sup-tRNA
…sans modifier le génome, modifier son expression !
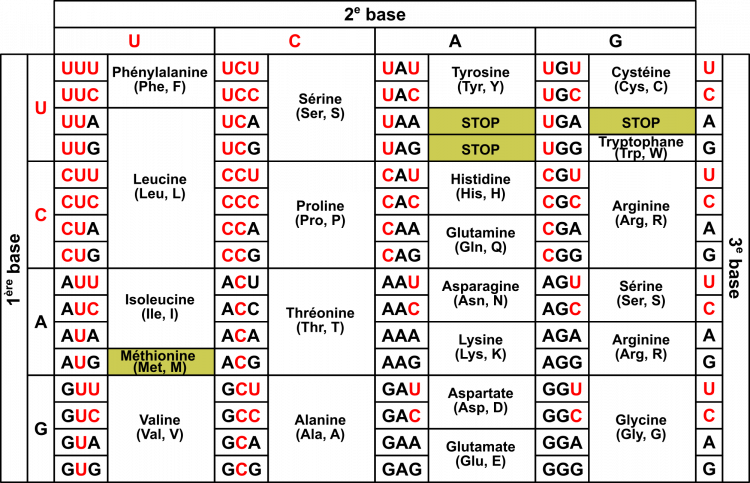
Dans une News and Views de Nature au titre malicieusement formulé — "Stop the nonsense: genome editing creates potentially therapeutic transfer RNAs" — Keeling (2025) (ici), présente le travail de Pierce et al. (2025) (ici), qui ouvre une piste thérapeutique pour toute une classe de maladies rares. Plus de 7 000 maladies rares sont connues, mais seules environ 5 % disposent d'un traitement. Parmi les variants pathogènes, une proportion non négligeable correspond à des mutations « non-sens » : une mutation transforme un codon ordinaire en codon stop prématuré (voir le tableau de la fig. 1 ci-contre), ce qui interrompt trop tôt la synthèse de la protéine. La stratégie testée ici consiste à faire lire malgré tout ce stop anormal pour obtenir une protéine de longueur complète. Reste qu'une protéine de longueur complète n'est pas forcément une protéine normale : l'acide aminé inséré à la place du stop peut en modifier la structure et en altérer la fonction. Malgré cette limite, une récupération même partielle de la fonction peut déjà suffire à atténuer certaines maladies graves. À ce stade, toutefois, la méthode ne vise qu'un seul type de codon stop prématuré, UAG, et pas encore UAA ni UGA. ![]() encourage le lecteur à aller vérifier dans l'article d'origine : ici
encourage le lecteur à aller vérifier dans l'article d'origine : ici
Cette technique montre bien que les ARNt détiennent la clé du code
Principe d'action de cette piste thérapeutique
L'idée générale de Pierce et al. (2025) est de faire lire malgré tout un codon stop prématuré afin de permettre la production d'une protéine de longueur complète. Il ne s'agit donc pas de corriger le gène muté lui-même, mais de modifier l'anticodon d'un ARNt endogène pour le transformer en ARNt suppresseur capable de relire un codon stop prématuré et d'insérer un acide aminé à la place du signal d'arrêt. Cela ne garantit toutefois ni une structure correcte, ni une stabilité normale, ni une pleine fonctionnalité de la protéine produite. Comme seuls les tissus ou le vecteur a été introduit sont modifiés, et que les codons stop normaux sont mieux protégés que les stops prématurés, l'approche n'entraîne pas une lecture anarchique de l'ensemble des signaux d'arrêt.
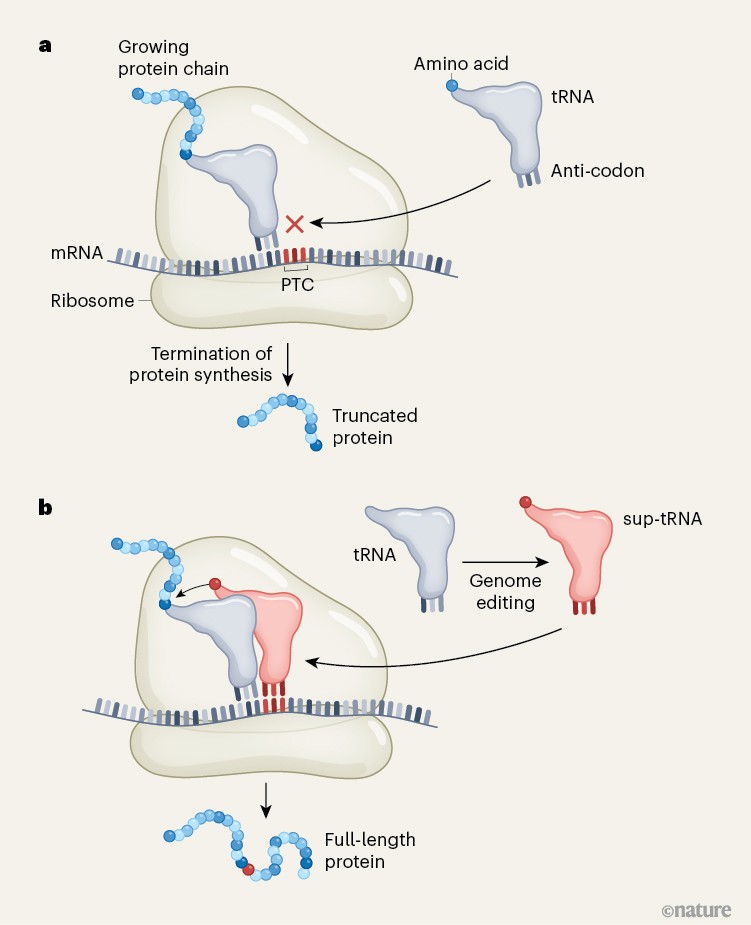
Figure 2 | principe d'action des ARNt suppresseur. a, Dans les cellules, la synthèse des protéines a lieu lorsque la machinerie ribosomique décode la séquence d'un ARN messager afin de déterminer quel acide aminé doit être ajouté ensuite à une chaîne protéique en cours d'élongation, portée par un ARN de transfert. De nombreuses variantes génétiques contiennent des codons de terminaison prématurée (PTC) — des triplets de nucléotides qui, une fois transcrits en ARN messager, interrompent la synthèse de la protéine avant que celle-ci n'ait atteint sa longueur complète.
b, Pierce et al. ont utilisé une technique d'édition du génome pour transformer des ARNt naturellement exprimés en ARNt suppresseurs (sup-tRNAs), capables de reconnaître un type particulier de PTC. Pendant la synthèse de la protéine, ce sup-ARNt se fixe sur le PTC et ajoute un acide aminé à la chaîne protéique. Cela permet à la synthèse de se poursuivre au-delà du PTC et d'aboutir à une protéine de longueur complète. De tels sup-ARNt présentent un potentiel thérapeutique pour des maladies associées à des variantes génétiques contenant des PTC. Source Kim Keeling (2025). (ici).
Mecanisme d'action de cette piste thérapeutique
Keeling (2025) indique que Pierce et al. (2025) ont identifié un ARNt suppresseur particulièrement actif contre un type précis de codon stop prématuré, UAG, puis l'ont testé dans des cellules humaines et chez la souris. Dans des lignées cellulaires porteuses de variants pathogènes, ils observent une restauration allant de 20 à 70 % de la fonction protéique normale. Dans un modèle murin de mucopolysaccharidose de type I, ils obtiennent jusqu'à 8 % d'activité normale de l'enzyme déficiente, ce qui suffit à atténuer plusieurs manifestations de la maladie. Ils rapportent aussi peu d'effets hors cible détectables et aucune lecture indésirable des codons stop normaux. Enfin, un criblage à grande échelle suggère que cette stratégie pourrait fonctionner dans de nombreux contextes moléculaires impliquant le codon UAG, y compris pour certains variants du gène CFTR, responsable de la mucoviscidose.Une exigence essentielle pour cette technique, comme pour les autres approches thérapeutiques fondées sur la suppression du non-sens, est d'obtenir une restauration cliniquement pertinente de la fonction de la protéine cible. Pierce et al. rapportent qu'une restauration allant jusqu'à 8 % de la fonction normale de la protéine a suffi à atténuer les symptômes dans un modèle murin de MPS I, une maladie pour laquelle moins de 1 % de la fonction normale suffit déjà à réduire nettement les manifestations cliniques. En revanche, un tel niveau serait insuffisant pour de nombreuses maladies génétiques nécessitant un seuil de correction plus élevé. Il faudra donc encore améliorer l'efficacité et la puissance des sup-ARNt utilisés pour la suppression du non-sens.
Même si les résultats de Pierce et de ses collègues suggèrent que cette approche par sup-ARNt pourrait avoir une large applicabilité, il faut garder à l'esprit que l'acide aminé inséré dans une chaîne protéique lors de la lecture au-delà d'un PTC peut avoir un effet important sur la stabilité et la fonction de la protéine. Il est donc peu probable que ce sup-ARNt permette de restaurer une fonction optimale pour toutes les protéines codées par des variants contenant un UAG. Des travaux supplémentaires seront nécessaires pour développer des sup-ARNt optimisés capables de permettre la lecture au-delà d'autres PTC, par exemple les codons UAA et UGA.
Mécanisme de prime editing ?
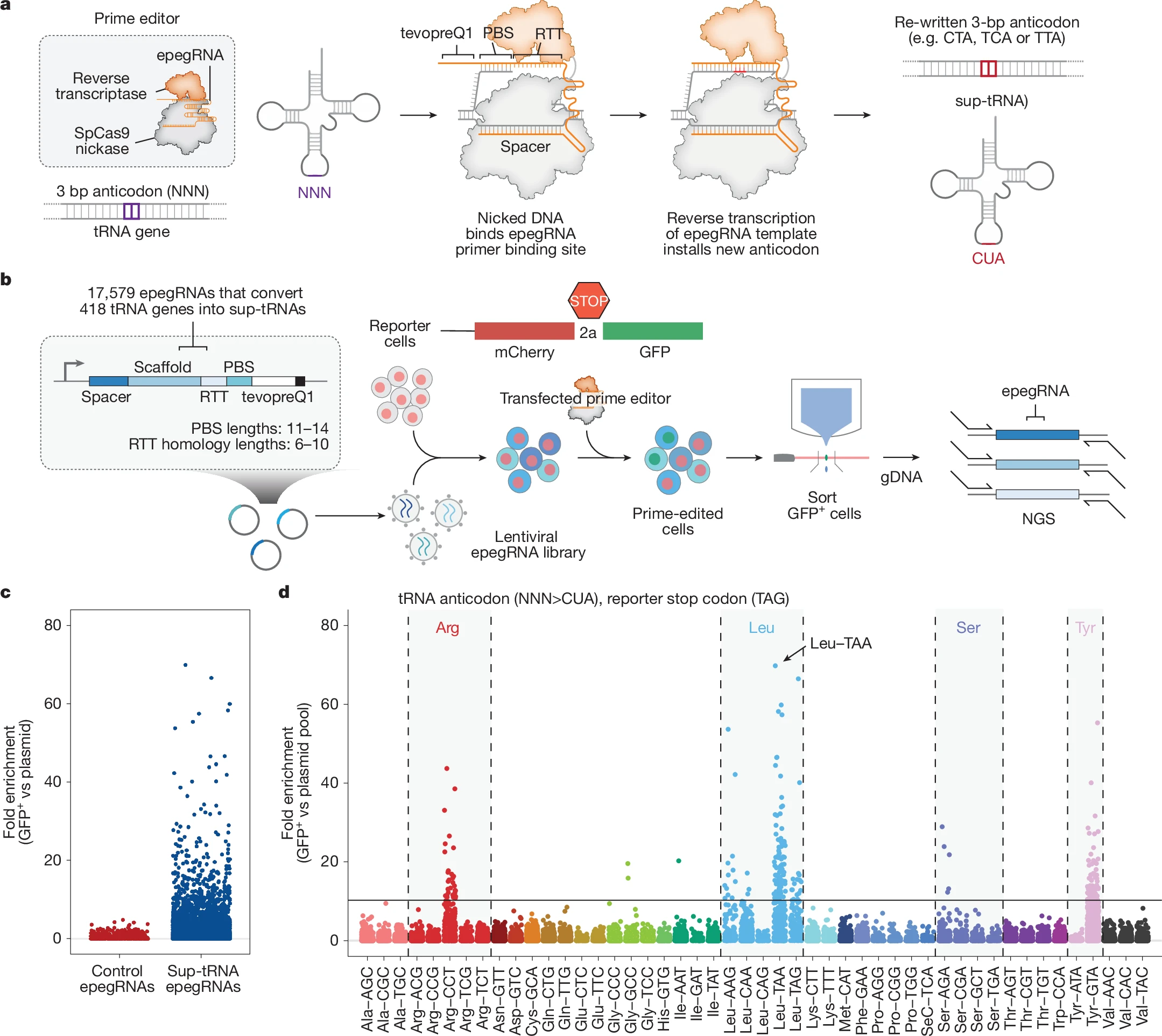
Le prime editing est utilisé ici comme un outil de "réécriture ciblée" : non pas pour corriger le gène muté, mais pour modifier l'anticodon d'un ARNt endogène et le transformer en ARNt suppresseur capable de relire un codon stop prématuré.
Pour approfondir voir Anzalone, & al. (2019).. ici:
Concrètement, Pierce et al. ciblent la boucle anticodon de gènes d'ARNt endogènes et remplacent l'anticodon natif par un anticodon suppresseur — par exemple CUA, UCA ou UUA — afin de reconnaître respectivement les codons stop TAG, TGA ou TAA. ![]() encourage le lecteur à aller vérifier dans l'article d'origine : ici
encourage le lecteur à aller vérifier dans l'article d'origine : ici
From: Prime editing-installed suppressor tRNAs for disease-agnostic genome editing
Références:
- Anzalone, A. V., Randolph, P. B., Davis, J. R., Sousa, A. A., Koblan, L. W., Levy, J. M., Chen, P. J., Wilson, C., Newby, G. A., Raguram, A., & Liu, D. R. (2019). Search-and-replace genome editing without double-strand breaks or donor DNA. Nature, 576(7785), 149‑157. https://doi.org/10.1038/s41586-019-1711-4
- Keeling, K. M. (s. d.). Transfer RNAs edited for 'non-stop' gene therapy: Transfer RNAs edited for 'non-stop' gene therapy. nature, 648(8092). Consulté 25 mars 2026, à l'adresse https://www.nature.com/articles/d41586-025-03587-3.pdfKeeling, K. M. (2025). Stop the nonsense : Genome editing creates potentially therapeutic transfer RNAs. Nature, 648(8092), 43‑45. https://doi.org/10.1038/d41586-025-03587-3Pierce, S. E., Erwood, S., Oye, K., An, M., Krasnow, N., Zhang, E., Raguram, A., Seelig, D., Osborn, M. J., & Liu, D. R. (2025). Prime editing-installed suppressor tRNAs for disease-agnostic genome editing. Nature, 648(8092), 191‑202. https://doi.org/10.1038/s41586-025-09732-2


Aucun commentaire:
Enregistrer un commentaire